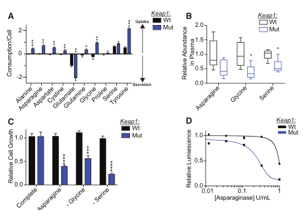
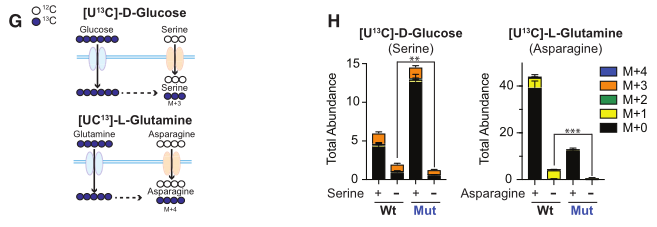
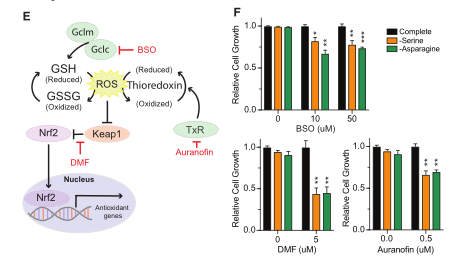
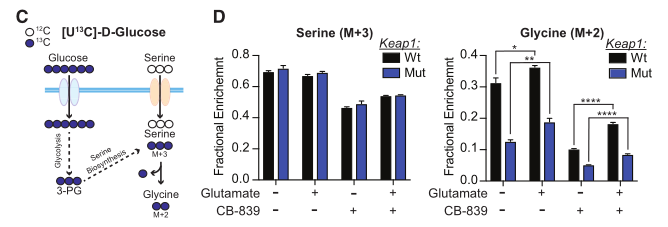
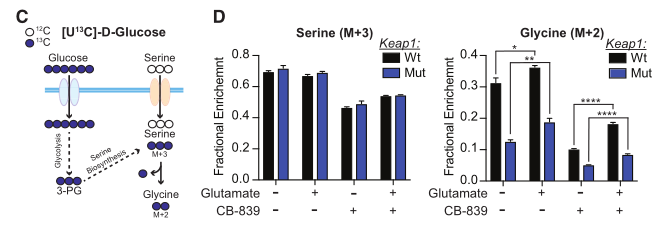
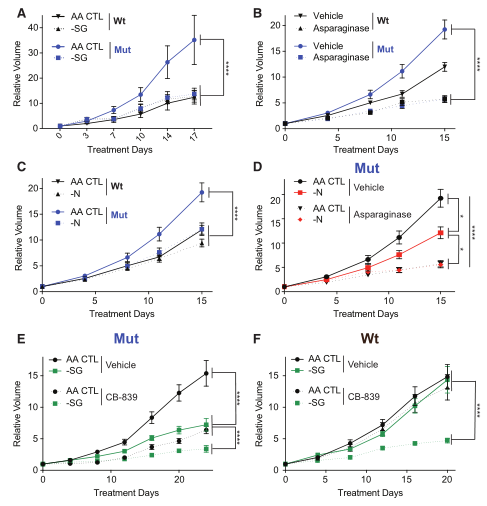
代谢重编程是肿瘤的一个标志现象,越来越多的证据表明细胞代谢的重编程支持了肿瘤的发生、进展、转移和耐药。近年随着代谢组学技术的发展,尤其是代谢流技术,极大的提升了对于肿瘤代谢异质性的理解。在此基础上,研究者们针对肿瘤新陈代谢提出了相关的治疗策略,如饮食控制、代谢酶抑制/激活等,也已经取得了积极的进展。 2020年2月,来自纽约大学医学院的研究团队在Cell metabolism(IF 27.3)发表题为“Activation of Oxidative Stress Response in Cancer Generates a Druggable Dependency on Exogenous Non-essential Amino Acids”的报道,研究者团队主要利用代谢流技术,阐明了Keap1突变型肿瘤中因代谢重编程发生的外源非必需氨基酸(NEAAs)依赖性的机制,及其对于肿瘤发生发展的意义,提出并验证了潜在的靶向代谢治疗策略。 研究材料 细胞、小鼠模型 技术路线 步骤1:利用代谢组及代谢流描绘代谢重编程表型; 步骤2:阐明验证发生机制及靶点挖掘; 步骤3:提出代谢靶向治疗策略。 研究结果 1. 研究背景介绍 NFE2L2(简称Nrf2)是细胞抗氧化反应的主要转录调节因子,控制过多条参与活性氧(ROS)解毒的基因转录。在正常情况下,Nrf2被隔离在细胞质中,通过与Kelch-like ECH-associated protein 1(简称Keap1)互作,不显示活性。当细胞中ROS积累,Keap1构象变化,Nrf2移位到细胞核促进相关靶基因转录。在KRAS驱动的非小细胞肺癌(NSCLC)中,大约20%的类型存在Keap1或Nrf2突变,是主要的治疗靶点。此外,Keap1/NRF2抗氧化信号通路的突变在几种实体癌症中是常见的事件,通常均与患者的不良预后有关。 2. 代谢重编程表型描绘 研究者在体内及体外实验中发现Keap1突变型肿瘤对外源NEAAs的摄取增多,尤其是当天冬氨酸、丝氨酸、甘氨酸这三种外源NEAAs耗尽时,Keap1突变型肿瘤出现明显的生长抑制现象,但WT型肿瘤细胞并未受到影响,研究者推测这一现象可能是Keap1突变后肿瘤细胞出现代谢重编程,导致对NEAAs的需求增加或者合成NEAAs的能力减弱,从而产生了对外源NEAAs的依赖性。 图1 外源丝氨酸、甘氨酸和天冬氨酸耗尽后出现显著生长抑制 使用[U-13C]glucose和[U-13C]glutamine作为同位素底物标记细胞后,通过代谢流技术对氨基酸合成相关通路进行分析,发现两种肿瘤对于丝氨酸的合成速率几乎一致,但Keap1突变型细胞中的丝氨酸含量几乎是WT肿瘤细胞的3倍,绝大部分来自外源。另外,Keap1突变型细胞中天冬酰胺几乎都依靠外源摄入。以上结果说明相比WT细胞,Keap1突变型肿瘤内部经过代谢重编程后,对于NEAAs需求量增大,同时合成能力不足以支持这种需求,这与产生外源NEAAs依赖性表型是一致的。 图2 代谢流分析氨基酸合成通路及内外源组成比例 3. 代谢重编程机制讨论及靶点挖掘 (1)重编程意义讨论及机制验证 研究者通过激活Nrf2和给予细胞高氧化环境等手段,证明对外源NEAAs的依赖性由Nrf2激活所引导,是一种针对肿瘤细胞内部高ROS积累环境的适应机制,当处于外源NEAAs耗尽环境时,Keap1突变型细胞会出现明显生长抑制。 图3 Nrf2介导的氧化应激作用 (2)靶点挖掘 谷氨酸是NEAAs合成通路上的重要节点代谢物,结合已有研究与实验验证,研究者首先确认了Keap1突变型细胞生长受到细胞内谷氨酸含量的调控。 另一方面Keap1突变型细胞展现出对外源丝氨酸缺乏的敏感性,研究者讨论了丝氨酸缺乏对于肿瘤细胞生长的抑制机制,发现核苷酸合成受阻是主要限制了Keap1突变细胞生长的主要原因。 为了探索Keap1突变型细胞内丝氨酸缺乏的原因,研究者用[U-13C]glucose标记Keap1突变型细胞,使用代谢流检测当丝氨酸耗尽时,从头合成通路的流量,发现相比WT细胞,Keap1突变型细胞中TCA循环的葡萄糖流量没有增加,另外谷氨酰胺进入TCA循环的流量也没有变化,表明Keap1突变型细胞中糖酵解相关前体的可用性没有减少。 图4 代谢流揭示丝氨酸合成通路流量变化 丝氨酸合成另一个关键节点是由谷氨酸与磷酸羟基丙酮酸(PHP)经催化,生成丝氨酸。这种转氨基反应是由磷酸丝氨酸转氨酶(PSAT)催化的。研究者在丝氨酸缺乏的情况下,向Keap1突变型细胞提供谷氨酸,发现细胞生长速率获得恢复。通过构建PSAT基因敲除的WT和Keap1突变肿瘤细胞,验证了这种能力依赖于PSAT的存在。 使用[α-15N] glutamine标记细胞,以确定谷氨酸氨基的代谢流向。发现外源丝氨酸耗尽时,细胞中增加15N标记的丝氨酸和甘氨酸比例上升。此外,还发现在缺乏丝氨酸的条件下,Keap1突变型细胞中15N标记的掺入减少,这表明Keap1突变细胞中谷氨酸可获得性的降低减少了丝氨酸的合成。用Nrf2的小分子激活剂处理Keap1 WT细胞,同样导致15N标记在丝氨酸和甘氨酸中的掺入减少。这证明在Keap1突变型细胞中丝氨酸的合成受到谷氨酸含量的调控,可以通过补充谷氨酸来恢复丝氨酸的合成。 图5 谷氨酸含量下降引发丝氨酸、甘氨酸合成减慢 4. 针对代谢异质性的潜在治疗策略 在上述基础上,针对代谢异质性,研究者提出了两种靶向代谢治疗策略,一种是利用肿瘤细胞对丝氨酸、甘氨酸的敏感性,设计了丝氨酸和甘氨酸饮食摄入限制、天冬酰胺饮食限制、天冬酰胺酶注射等三种干预策略,通过动物模型验证发现以上策略均能明显抑制Keap1突变型肿瘤生长,其中使用天冬酰胺酶注射+天冬酰胺饮食限制联合策略会强烈抑制肿瘤生长,但WT型肿瘤细胞对这三种策略不敏感。 另一种是针对肿瘤对于谷氨酸缺乏的敏感性设计的策略,其中谷氨酰胺酶抑制剂CB-839和丝氨酸及甘氨酸饮食摄入限制联合治疗显著抑制了Keap1突变型肿瘤的生长,但令人惊喜的是,WT肿瘤的生长同样受到该策略的强烈抑制。 图6 靶向治疗策略验证 小结 研究者描述了肿瘤细胞发生代谢重编程后,产生对外源非必需氨基酸依赖的机制及意义,并确认谷氨酸和丝氨酸是重要的调节靶点,通过干预肿瘤可摄取的关键氨基酸量,成功控制了肿瘤生长。 中科优品推荐 【中科新生命】可提供代谢流+全谱代谢组代谢重编程研究一站式解决方案,现全谱非靶向代谢组火热促销中,欢迎感兴趣的老师前来咨询。


Cell Metabolism(IF 27.3)| 饥饿疗法,代谢流助力揭示肿瘤的代谢脆弱性
作者:上海中科新生命生物科技有限公司 2021-12-31T15:17 (访问量:2227)
上海中科新生命生物科技有限公司 商家主页
地 址: 上海市园美路58号1号楼15-18楼
联系人: 徐
电 话: 021-54665263
传 真:
Email:marketing@aptbiotech.com
相关咨询
会议邀请 | 第8届全国植物蛋白质研究大会暨首届贵阳生命科学新高地科学家论坛 (2023-07-07T14:37 浏览数:13747)
项目文章Cell(IF 64.5)| 中国科技大学探索食物过敏谜团 (2023-07-07T14:22 浏览数:13908)
Gastroenterology(IF 29.4)| 基于机器学习算法开发的外泌体miRNA生物标志物用于胰腺导管腺癌早期诊断 (2023-07-05T15:54 浏览数:11542)
Cancer Letters(IF 9.7)|天津市环湖医院利用Labelfree揭示超声-替莫唑胺联合诱导胶质瘤细胞的凋亡机制 (2023-06-30T09:37 浏览数:12577)
Excel表免费下载 | 速来围观!2023年影响因子发布 (2023-06-29T09:35 浏览数:11332)
外泌体多组学创新解决方案,精准、前沿的疾病诊断生物标志物 (2023-06-28T10:20 浏览数:15524)
Immunity (IF=43.474)丨单细胞+空间联合揭示肉芽肿形成的异常淋巴发育进程 (2023-06-26T17:28 浏览数:11688)
专家齐聚 亮点回顾 | 2023年海口·中医药创新多组学研究论坛圆满落幕 (2023-06-25T10:10 浏览数:16239)
项目文章Plant J(IF 7)| 杭州师范大学王慧中团队通过空间代谢+单细胞测序等揭示红豆杉幼茎细胞特异的紫杉烷合成调控模式 (2023-06-25T09:42 浏览数:13815)
项目文章Gut Microbes(IF 9.434)| 肠道微生物竟是导致胆囊切除术后患者腹泻的元凶? (2023-06-14T16:35 浏览数:11237)
